
Реконструкция молочной железы DIEP-лоскутом при раке молочной железы
ВВЕДЕНИЕ
Рак молочной железы (РМЖ) сохраняет лидерство среди злокачественных заболеваний у женщин во всем мире и остается одной из наиболее важных медицинских и социально-экономических проблем. По данным литературы ежегодно в мире регистрируется более 2,26 млн случаев РМЖ, что составляет 11,7% всех злокачественных новообразований у лиц обоего пола. В России в 2020 г. абсолютное число случаев РМЖ составило 65 468 (11,8% в структуре общей заболеваемости раком). Государственные программы по развитию оказания онкологической помощи населению России позволили усовершенствовать скрининг и диагностику РМЖ, что привело к выявлению заболевания на ранних стадиях, что соответствует общемировой тенденции.
Современный тренд в развитии реконструктивной хирургии при РМЖ сподвигнул к образованию школ по обучению специалистов в данной области и открытию в последующем специализированных реконструктивных отделений. Сегодня невозможно представить современное онкологическое отделение, где выполняют операции на молочной железе при РМЖ без реконструктивного компонента. В западных странах практически каждая женщина просыпается после операции на молочной железе по поводу РМЖ уже с тем или иным реконструктивным компонентом. В редких случаях пациентка покидает клинику после мастэктомии без варианта реконструкции, а возросший процент и уровень органосохраняющих операций достиг максимального эстетического эффекта с развитием онкопластических методик. Несмотря на это, в 70% случаев выполнение радикальной мастэктомии (РМЭ) в связи с противопоказанием к сохранению молочной железы и неудовлетворительными результатами эстетических органосохранных операций продолжает оставаться часто выполняемой операцией.
Восстановление молочной железы при РМЖ может осуществляться одномоментно или в отсроченном варианте, этапность определяется хирургом совместно с пациенткой в зависимости от планируемого дальнейшего лечения, конститутивных особенностей и сопутствующей патологии. В арсенале хирурга существуют различные варианты реконструкции молочной железы, наиболее часто восстановление осуществляется с помощью имплантатов, собственными тканями — лоскутами передней брюшной стенки (TRAM, DIEP), либо комбинацией имплантатов с собственными тканями (широчайшей мышцы спины — TDL).
Реконструкция молочной железы — это сложный многоэтапный процесс, требующий слаженных действий со стороны хирурга и со стороны пациентки. Нередко реконструктивный этап сопряжен с развитием осложнений, которые даже могут приводить к фатальным последствиям в виде потери имплантата или лоскута. По данным разных источников при реконструкции имплантатами риск осложнений с потерей имплантатов может достигать 30–52%. Изначально прогнозируя эти возможные неудачи, мы можем этим пациенткам рекомендовать реконструкцию DIEP- лоскутом. В тех случаях, когда планируется лучевая терапия, у женщины высокий индекс массы тела (ИМТ) или же низкий пинч-тест, мы можем смело изначально рекомендовать DIEP-реконструкцию.
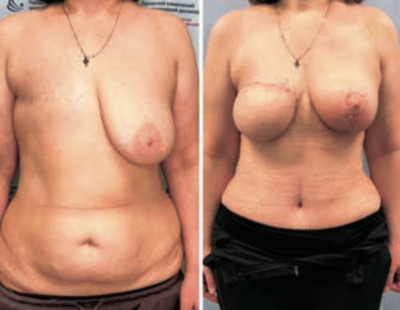
Осложнения, возникшие при восстановлении молочной железы лоскутами, отличаются своей спецификой, могут быть связаны как с донорской областью, откуда берется материал для восстановления, так и с реципиентной зоной, куда лоскут помещается, а любая неудача в этом процессе сопряжена с более тяжелым периодом восстановления и снижением психоэмоционального фона пациентки. В некоторых случаях мы можем с этими осложнениями успешно справиться и достичь окончательного стабильного эстетического результата, а иногда даже их предотвратить, выбрав оптимальный вариант реконструкции для конкретной пациентки.
Не обладая необходимыми навыками для выполнения операций по всем вариантам реконструкций молочной железы или при отсутствии условий для выполнения этих операций мы заведомо повышаем риск возможных осложнений в будущем. К примеру, женщине, которой показана реконструкция молочной железы с помощью микрохирургической техники и пересадки DIEP-лоскута, устанавливается имплантат, не оставляя выбора для пациентки и выполнения пластики в свободном варианте. Это не означает, что при реконструкции молочной железы DIEP- лоскутом не будет осложнений, но, возможно, в данном случае их процент будет минимальным и будет достигнут удовлетворительный эстетический результат.
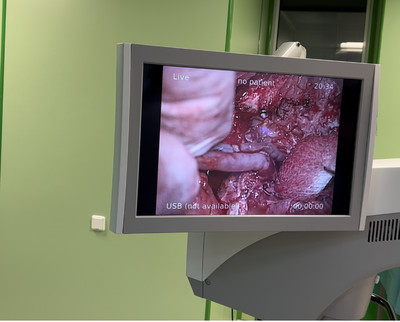
На определенном этапе своей хирургической практики мы столкнулись с такой проблемой, когда некоторой группе пациенток требовалась DIEP-реконструкция, так как другие варианты не приносили должного эстетического результата или возникали осложнения, которые можно было исправить исключительно с применением микрохирургии. Нам пришлось пройти различные этапы обучения и становления в выполнении микрохирургических операций, для того чтобы решить эти проблемы и выполнять данной группе пациенток реконструкцию молочной железы с помощью DIEP-лоскута.
ЦЕЛЬ ИССЛЕДОВАНИЯ: оценить эффективность и эстетическую приемлемость применения DIEP-лоскута у пациенток с осложнениями после реконструкции молочных желез имплантатами/экспандерами в анамнезе и высокими факторами риска осложнений.
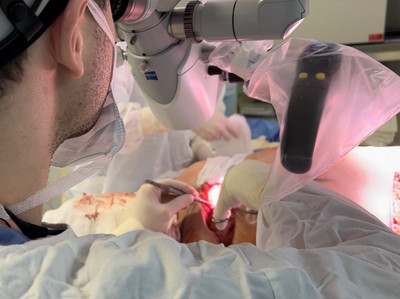
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проводилось на базе Санкт- Петербургского государственного учреждения здравоохранения «Городской клинический онкологический диспансер» в отделении опухолей молочной железы No 2. С февраля 2022 по декабрь 2023 г. выполнено 20 отсроченных реконструкций молочных желез с использованием лоскута на перфоранте нижней глубокой эпигастральной артерии (DIEP-лоскут) у пациенток, ранее прошедших радикальное лечение. Время наблюдения после прошедшего радикального лечения составило более 12 месяцев.
Основные критерии отбора: осложнения после реконструкций имплантатами/экспандерами молочных желез, лучевая терапия в анамнезе, пинч-тест менее 1 см, избыток тканей передней брюшной стенки, наличие доминантных перфорантных сосудов бассейна нижней эпигастральной артерии. Абсолютным противопоказанием к проведению DIEP-реконструкции являлось отсутствие доминантного перфоранта из-за «рассыпного» типа кровоснабжения данной области. Для предоперационной разметки лоскута применялись компьютерная томография (КТ) в ангиорежиме органов грудной клетки и брюшной полости на аппарате Philips Ingenuity Elite и ультразвуковая допплерография при помощи слепого допплера Edan SD3.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Средняя длительность операции составила 447 мин (7,45 ч). Средний возраст пациенток составил 48 лет (минимальный возраст — 36 лет, максимальный возраст — 56 лет). Медиана наблюдения составила 9,3 месяца. За период наблюдения рецидивов и прогрессирования заболевания не было выявлено.
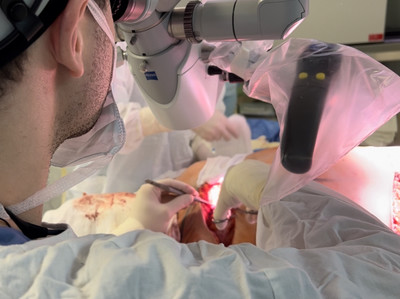
Все женщины распределились следующим образом: 7 пациенток после экспандерной дермотензии, у которых на фоне лучевой терапии развилась отрицательная дермотензия с продавливанием реберных дуг, 5 пациенток с про- трузией имплантата и инфекционными осложнениями в послеоперационном периоде в анамнезе, 3 больных анамнестически с протрузией экспандера в послеоперационном периоде, 5 пациенток после радикальной мастэктомии и лучевой терапии.
Из 20 обследованных у 4 (20%) был сахарный диабет 2-го типа. Средний индекс массы тела составил 30,5 (стандартное отклонение ±4,2). У одной пациентки был длительный анамнез курения (более 10 лет). Также были включены женщины, у которых имелись оперативные вмешательства на передней брюшной стенке: 5 — кесарево сечение, 2 — лапароскопическая холецистэктомия, 1 — аппендэктомия, 1 — два сеанса липосакции. У 7 пациенток была проведена химиотерапия антрациклинами и таксанами в анамнезе.
Также отмечено, что пациентки с ИМТ от 30,0 до 35кг/м2 и 35кг/м2 или выше подвергались значительно большему риску осложнений по сравнению с пациентками с нормальным ИМТ (от 18,5 до 25 кг/м2).
Суммарный процент осложнений составил 35%. Доминантным осложнением была длительная серома в донорской зоне — 3 случая (15%), все пациентки с серомами имели ожирение I–II степени. Серьезное осложнение, которое привело к полной потере лоскута,— недостаточный венозный отток — отмечено в 1 случае (5%) с отягощенным анамнезом (ожирение III степени, лучевая терапия). Частичный некроз лоскута менее 20% был выявлен у 1 (5%) обследуемой, впоследствии зажил вторичным натяжением. Ранняя послеоперационная гематома выявлена у 1 (5%) пациентки, которой потребовалось экстренное хирургическое вмешательство, без потери и частичного некроза лоскута. Послеоперационная вентральная грыжа сформировалась у 1 (5%) пациентки с оперативными вмешательствами на передней брюшной стенке в анамнезе (аппендэктомия).
Не отмечено статистически значимой разницы в количестве осложнений в разных возрастных группах.
При оценке влияния лучевой терапии в анамнезе на количество осложнений было выявлено, что из 7 пациенток с послеоперационными осложнениями 5 женщин ранее проходили лучевую терапию. Различия статистически значимы.
Не было отмечено влияния химиотерапии в анамнезе на количество осложнений реконструкции.
Для достижения симметрии молочных желез всем пациенткам при необходимости выполнялась симметризирующая мастопексия контралатеральной молочной железы. Итого из 20 пациенток 8 была выполнена симметризирующая мастопексия.
Оценка косметических результатов проводилась с помощью опросника Breast Q Reconstruction Module Pre- and Postoperative Scales версия 2.0. При оценке модуля «Удовлетворенность молочной железой до и после операции» средний балл составил 51 до лечения и 75 после, в модуле «Удовлетворенность результатом реконструкции» средний балл оставил 72.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
По данным ряда авторов частота послеоперационных осложнений при реконструкциях молочной железы имплантатами/экспандерами варьируется от 5,8% до 52%, а при реконструкции аутологичными тканями достигает 46,9%. При этом, если рассматривать конкретные осложнения, связанные с имплантатами (некроз краев раны, инфекционные осложнения, серомы, гематомы, капсулярные контрактуры, разрыв или ротация имплантата), то можно отметить, что большая часть данных осложнений приводит либо к потере имплантата, либо к повторным операциям. В то время как вмешательства с использованием аутологичных тканей требуют реопераций либо при полной потере лоскута, либо при частичной потере лоскута >20%. При этом частота полной потери лоскута составляет от 1 до 5%. В нашем исследовании случилась одна потеря лоскута, что составило 5%, при достаточно маленькой выборке (n=20), и потребовалась всего одна реоперация для достижения приемлемого косметического результата.
Среди демографических переменных возраст не является противопоказанием к реконструкции имплантатами/экспандерами или аутологичными лоскутами. Многоцентровой ретроспективный анализ по оценке результатов аутологичных реконструкций у 1809 пациенток и реконструкций имплантатами/экспандерами у 1170 пациенток привел к выводу, что осложнения в возрастных группах старше 65 лет были эквивалентны таковым в группе более молодых женщин.
В нашем анализе было замечено, что тяжелее всего реконструкции молочной железы переносили пациентки с ИМТ более 30 кг/м2. Данный вывод не является новым, так как ранее публиковались результаты анализа 15937 пациенток, сообщающие, что ожирение II и III степени является важным предиктором осложнений при реконструкции молочной железы.
При анализе частоты осложнений после проведенной химиотерапии в анамнезе не было выявлено существенного влияния на количество осложнений, что подтверждается результатами более ранних исследований. Однако лучевая терапия статистически доказано влияла на количество осложнений в послеоперационном периоде.
При оценке косметических результатов с помощью шкалы Breast-Q нами был получен достаточно высокий косметический результат (72 балла), что свидетельствует об эффективности применения DIEP-лоскута у определенной группы больных.
ВЫВОДЫ
Применение DIEP-лоскута с осложнениями у пациенток после реконструкции молочных желез имплантатами/экспандерами в анамнезе и высокими факторами риска осложнений является эффективным и безопасным методом реконструкции молочной железы с хорошим косметическим результатом.
Сведения об авторах:
Топузов Эльдар Эскендерович — доктор медицинских наук, профессор, заведующий кафедрой госпитальной хирургии им. В.А.Оппеля, федеральное государственное бюджетное образовательное учреждение высшего образования «Северо-Западный государственный медицинский университет им. И. И. Мечникова» Министерства здравоохранения Российской Федерации; главный врач Санкт-Петербургского государственного бюджетного учреждения здравоохранения «Городской клиниче- ский онкологический диспансер».
Скворцов Виталий Александрович — кандидат медицинских наук, врач-онколог, пластический хирург, доцент кафед- ры онкологии федерального государственного бюджетного образовательного учреждения высшего образования «Санкт-Петербургский государственный университет» Правительства Российской Федерации; заведующий отделением опухолей молочной железы (хирургических методов лечения) No 2 Санкт-Петербургского государственного бюджетного учреждения здравоохранения «Городской клинический онкологический диспансер».
Гор Людмила Андреевна — врач-онколог, пластический хирург отделения опухолей молочной железы (хирургических методов лечения) No 2 Санкт-Петербургского государственного бюджетного учреждения здравоохранения «Городской клинический онкологический диспансер».
Колчанов Георгий Михайлович — врач-онколог, пластический хирург отделения No 8 Санкт-Петербургского государственного бюджетного учреждения здравоохранения «Городской клинический онкологический диспансер».
Рак молочной железы (РМЖ) сохраняет лидерство среди злокачественных заболеваний у женщин во всем мире и остается одной из наиболее важных медицинских и социально-экономических проблем. По данным литературы ежегодно в мире регистрируется более 2,26 млн случаев РМЖ, что составляет 11,7% всех злокачественных новообразований у лиц обоего пола. В России в 2020 г. абсолютное число случаев РМЖ составило 65 468 (11,8% в структуре общей заболеваемости раком). Государственные программы по развитию оказания онкологической помощи населению России позволили усовершенствовать скрининг и диагностику РМЖ, что привело к выявлению заболевания на ранних стадиях, что соответствует общемировой тенденции.
Современный тренд в развитии реконструктивной хирургии при РМЖ сподвигнул к образованию школ по обучению специалистов в данной области и открытию в последующем специализированных реконструктивных отделений. Сегодня невозможно представить современное онкологическое отделение, где выполняют операции на молочной железе при РМЖ без реконструктивного компонента. В западных странах практически каждая женщина просыпается после операции на молочной железе по поводу РМЖ уже с тем или иным реконструктивным компонентом. В редких случаях пациентка покидает клинику после мастэктомии без варианта реконструкции, а возросший процент и уровень органосохраняющих операций достиг максимального эстетического эффекта с развитием онкопластических методик. Несмотря на это, в 70% случаев выполнение радикальной мастэктомии (РМЭ) в связи с противопоказанием к сохранению молочной железы и неудовлетворительными результатами эстетических органосохранных операций продолжает оставаться часто выполняемой операцией.
Восстановление молочной железы при РМЖ может осуществляться одномоментно или в отсроченном варианте, этапность определяется хирургом совместно с пациенткой в зависимости от планируемого дальнейшего лечения, конститутивных особенностей и сопутствующей патологии. В арсенале хирурга существуют различные варианты реконструкции молочной железы, наиболее часто восстановление осуществляется с помощью имплантатов, собственными тканями — лоскутами передней брюшной стенки (TRAM, DIEP), либо комбинацией имплантатов с собственными тканями (широчайшей мышцы спины — TDL).
Реконструкция молочной железы — это сложный многоэтапный процесс, требующий слаженных действий со стороны хирурга и со стороны пациентки. Нередко реконструктивный этап сопряжен с развитием осложнений, которые даже могут приводить к фатальным последствиям в виде потери имплантата или лоскута. По данным разных источников при реконструкции имплантатами риск осложнений с потерей имплантатов может достигать 30–52%. Изначально прогнозируя эти возможные неудачи, мы можем этим пациенткам рекомендовать реконструкцию DIEP- лоскутом. В тех случаях, когда планируется лучевая терапия, у женщины высокий индекс массы тела (ИМТ) или же низкий пинч-тест, мы можем смело изначально рекомендовать DIEP-реконструкцию.

Осложнения, возникшие при восстановлении молочной железы лоскутами, отличаются своей спецификой, могут быть связаны как с донорской областью, откуда берется материал для восстановления, так и с реципиентной зоной, куда лоскут помещается, а любая неудача в этом процессе сопряжена с более тяжелым периодом восстановления и снижением психоэмоционального фона пациентки. В некоторых случаях мы можем с этими осложнениями успешно справиться и достичь окончательного стабильного эстетического результата, а иногда даже их предотвратить, выбрав оптимальный вариант реконструкции для конкретной пациентки.
Не обладая необходимыми навыками для выполнения операций по всем вариантам реконструкций молочной железы или при отсутствии условий для выполнения этих операций мы заведомо повышаем риск возможных осложнений в будущем. К примеру, женщине, которой показана реконструкция молочной железы с помощью микрохирургической техники и пересадки DIEP-лоскута, устанавливается имплантат, не оставляя выбора для пациентки и выполнения пластики в свободном варианте. Это не означает, что при реконструкции молочной железы DIEP- лоскутом не будет осложнений, но, возможно, в данном случае их процент будет минимальным и будет достигнут удовлетворительный эстетический результат.

На определенном этапе своей хирургической практики мы столкнулись с такой проблемой, когда некоторой группе пациенток требовалась DIEP-реконструкция, так как другие варианты не приносили должного эстетического результата или возникали осложнения, которые можно было исправить исключительно с применением микрохирургии. Нам пришлось пройти различные этапы обучения и становления в выполнении микрохирургических операций, для того чтобы решить эти проблемы и выполнять данной группе пациенток реконструкцию молочной железы с помощью DIEP-лоскута.
ЦЕЛЬ ИССЛЕДОВАНИЯ: оценить эффективность и эстетическую приемлемость применения DIEP-лоскута у пациенток с осложнениями после реконструкции молочных желез имплантатами/экспандерами в анамнезе и высокими факторами риска осложнений.

МАТЕРИАЛЫ И МЕТОДЫ
Исследование проводилось на базе Санкт- Петербургского государственного учреждения здравоохранения «Городской клинический онкологический диспансер» в отделении опухолей молочной железы No 2. С февраля 2022 по декабрь 2023 г. выполнено 20 отсроченных реконструкций молочных желез с использованием лоскута на перфоранте нижней глубокой эпигастральной артерии (DIEP-лоскут) у пациенток, ранее прошедших радикальное лечение. Время наблюдения после прошедшего радикального лечения составило более 12 месяцев.
Основные критерии отбора: осложнения после реконструкций имплантатами/экспандерами молочных желез, лучевая терапия в анамнезе, пинч-тест менее 1 см, избыток тканей передней брюшной стенки, наличие доминантных перфорантных сосудов бассейна нижней эпигастральной артерии. Абсолютным противопоказанием к проведению DIEP-реконструкции являлось отсутствие доминантного перфоранта из-за «рассыпного» типа кровоснабжения данной области. Для предоперационной разметки лоскута применялись компьютерная томография (КТ) в ангиорежиме органов грудной клетки и брюшной полости на аппарате Philips Ingenuity Elite и ультразвуковая допплерография при помощи слепого допплера Edan SD3.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Средняя длительность операции составила 447 мин (7,45 ч). Средний возраст пациенток составил 48 лет (минимальный возраст — 36 лет, максимальный возраст — 56 лет). Медиана наблюдения составила 9,3 месяца. За период наблюдения рецидивов и прогрессирования заболевания не было выявлено.

Все женщины распределились следующим образом: 7 пациенток после экспандерной дермотензии, у которых на фоне лучевой терапии развилась отрицательная дермотензия с продавливанием реберных дуг, 5 пациенток с про- трузией имплантата и инфекционными осложнениями в послеоперационном периоде в анамнезе, 3 больных анамнестически с протрузией экспандера в послеоперационном периоде, 5 пациенток после радикальной мастэктомии и лучевой терапии.
Из 20 обследованных у 4 (20%) был сахарный диабет 2-го типа. Средний индекс массы тела составил 30,5 (стандартное отклонение ±4,2). У одной пациентки был длительный анамнез курения (более 10 лет). Также были включены женщины, у которых имелись оперативные вмешательства на передней брюшной стенке: 5 — кесарево сечение, 2 — лапароскопическая холецистэктомия, 1 — аппендэктомия, 1 — два сеанса липосакции. У 7 пациенток была проведена химиотерапия антрациклинами и таксанами в анамнезе.
Также отмечено, что пациентки с ИМТ от 30,0 до 35кг/м2 и 35кг/м2 или выше подвергались значительно большему риску осложнений по сравнению с пациентками с нормальным ИМТ (от 18,5 до 25 кг/м2).
Суммарный процент осложнений составил 35%. Доминантным осложнением была длительная серома в донорской зоне — 3 случая (15%), все пациентки с серомами имели ожирение I–II степени. Серьезное осложнение, которое привело к полной потере лоскута,— недостаточный венозный отток — отмечено в 1 случае (5%) с отягощенным анамнезом (ожирение III степени, лучевая терапия). Частичный некроз лоскута менее 20% был выявлен у 1 (5%) обследуемой, впоследствии зажил вторичным натяжением. Ранняя послеоперационная гематома выявлена у 1 (5%) пациентки, которой потребовалось экстренное хирургическое вмешательство, без потери и частичного некроза лоскута. Послеоперационная вентральная грыжа сформировалась у 1 (5%) пациентки с оперативными вмешательствами на передней брюшной стенке в анамнезе (аппендэктомия).
Не отмечено статистически значимой разницы в количестве осложнений в разных возрастных группах.
При оценке влияния лучевой терапии в анамнезе на количество осложнений было выявлено, что из 7 пациенток с послеоперационными осложнениями 5 женщин ранее проходили лучевую терапию. Различия статистически значимы.
Не было отмечено влияния химиотерапии в анамнезе на количество осложнений реконструкции.
Для достижения симметрии молочных желез всем пациенткам при необходимости выполнялась симметризирующая мастопексия контралатеральной молочной железы. Итого из 20 пациенток 8 была выполнена симметризирующая мастопексия.
Оценка косметических результатов проводилась с помощью опросника Breast Q Reconstruction Module Pre- and Postoperative Scales версия 2.0. При оценке модуля «Удовлетворенность молочной железой до и после операции» средний балл составил 51 до лечения и 75 после, в модуле «Удовлетворенность результатом реконструкции» средний балл оставил 72.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
По данным ряда авторов частота послеоперационных осложнений при реконструкциях молочной железы имплантатами/экспандерами варьируется от 5,8% до 52%, а при реконструкции аутологичными тканями достигает 46,9%. При этом, если рассматривать конкретные осложнения, связанные с имплантатами (некроз краев раны, инфекционные осложнения, серомы, гематомы, капсулярные контрактуры, разрыв или ротация имплантата), то можно отметить, что большая часть данных осложнений приводит либо к потере имплантата, либо к повторным операциям. В то время как вмешательства с использованием аутологичных тканей требуют реопераций либо при полной потере лоскута, либо при частичной потере лоскута >20%. При этом частота полной потери лоскута составляет от 1 до 5%. В нашем исследовании случилась одна потеря лоскута, что составило 5%, при достаточно маленькой выборке (n=20), и потребовалась всего одна реоперация для достижения приемлемого косметического результата.
Среди демографических переменных возраст не является противопоказанием к реконструкции имплантатами/экспандерами или аутологичными лоскутами. Многоцентровой ретроспективный анализ по оценке результатов аутологичных реконструкций у 1809 пациенток и реконструкций имплантатами/экспандерами у 1170 пациенток привел к выводу, что осложнения в возрастных группах старше 65 лет были эквивалентны таковым в группе более молодых женщин.
В нашем анализе было замечено, что тяжелее всего реконструкции молочной железы переносили пациентки с ИМТ более 30 кг/м2. Данный вывод не является новым, так как ранее публиковались результаты анализа 15937 пациенток, сообщающие, что ожирение II и III степени является важным предиктором осложнений при реконструкции молочной железы.
При анализе частоты осложнений после проведенной химиотерапии в анамнезе не было выявлено существенного влияния на количество осложнений, что подтверждается результатами более ранних исследований. Однако лучевая терапия статистически доказано влияла на количество осложнений в послеоперационном периоде.
При оценке косметических результатов с помощью шкалы Breast-Q нами был получен достаточно высокий косметический результат (72 балла), что свидетельствует об эффективности применения DIEP-лоскута у определенной группы больных.
ВЫВОДЫ
Применение DIEP-лоскута с осложнениями у пациенток после реконструкции молочных желез имплантатами/экспандерами в анамнезе и высокими факторами риска осложнений является эффективным и безопасным методом реконструкции молочной железы с хорошим косметическим результатом.
Сведения об авторах:
Топузов Эльдар Эскендерович — доктор медицинских наук, профессор, заведующий кафедрой госпитальной хирургии им. В.А.Оппеля, федеральное государственное бюджетное образовательное учреждение высшего образования «Северо-Западный государственный медицинский университет им. И. И. Мечникова» Министерства здравоохранения Российской Федерации; главный врач Санкт-Петербургского государственного бюджетного учреждения здравоохранения «Городской клиниче- ский онкологический диспансер».
Скворцов Виталий Александрович — кандидат медицинских наук, врач-онколог, пластический хирург, доцент кафед- ры онкологии федерального государственного бюджетного образовательного учреждения высшего образования «Санкт-Петербургский государственный университет» Правительства Российской Федерации; заведующий отделением опухолей молочной железы (хирургических методов лечения) No 2 Санкт-Петербургского государственного бюджетного учреждения здравоохранения «Городской клинический онкологический диспансер».
Гор Людмила Андреевна — врач-онколог, пластический хирург отделения опухолей молочной железы (хирургических методов лечения) No 2 Санкт-Петербургского государственного бюджетного учреждения здравоохранения «Городской клинический онкологический диспансер».
Колчанов Георгий Михайлович — врач-онколог, пластический хирург отделения No 8 Санкт-Петербургского государственного бюджетного учреждения здравоохранения «Городской клинический онкологический диспансер».